All about multiple myeloma from def to prevention
Reading File
Finding Sources
Searching PubMed
"multiple myeloma"[MeSH Terms] AND "therapy"[MeSH Terms]
Searching the Web
multiple myeloma 2025 guidelines prevention treatment overview
Reading File
Reading File
Searching Images
multiple myeloma plasma cells bone marrow histology
Finding Sources
Reading File
Reading File
Reading File
Loading Image
Loading Image
Loading Image
I now have comprehensive content from multiple authoritative textbooks plus updated 2025 guideline information. Here is a complete, structured overview of multiple myeloma.
Multiple Myeloma — A Complete Overview
1. Definition
Multiple myeloma (MM) is a malignancy of clonal plasma cells that infiltrate the bone marrow, producing a monoclonal immunoglobulin (M protein) and causing systemic organ damage. It is formally defined by the simultaneous presence of:
- ≥10% clonal plasma cells on bone marrow examination, AND
- M protein in serum or urine (absent only in nonsecretory myeloma), AND
- One or more myeloma-defining events (MDE) — the CRAB criteria or high-risk biomarkers (see Diagnosis section)
It must be distinguished from its precursor states: MGUS (Monoclonal Gammopathy of Undetermined Significance) and Smoldering Multiple Myeloma (SMM).
— Goldman-Cecil Medicine, Chapter 173
2. Epidemiology
| Feature | Data |
|---|---|
| Proportion of all malignancies | ~1% |
| Proportion of hematologic malignancies | ~10–12% |
| New US cases/year | ~30,000–35,000 |
| Median age at diagnosis | 70 years |
| Sex | More common in males |
| Race | ~2× more frequent in people of African descent |
The disease is essentially rare under age 40. About one-third of patients with MGUS eventually progress to symptomatic myeloma over 10+ years.
— Goldman-Cecil Medicine; Robbins & Kumar Basic Pathology
3. Pathogenesis
Molecular Mechanisms
Myeloma arises from post-germinal center B cells (plasma cells) that have undergone somatic hypermutation and class-switch recombination. Key oncogenic events include:
- IgH translocations (chromosome 14q32) fusing IgH to oncogenes:
- t(11;14) → Cyclin D1 overexpression (most common, ~20%)
- t(4;14) → FGFR3 and MMSET (high-risk)
- t(14;16) → MAF oncogene (high-risk)
- Dysregulation of D cyclins → increased cell proliferation
- Trisomies (hyperdiploid myeloma, ~50%) — generally lower risk
- MYC translocations — appear late; associated with aggressive disease
- IL-6 produced by bone marrow stromal fibroblasts and macrophages drives proliferation and survival of myeloma cells
Bone Disease Mechanism
Myeloma cells upregulate RANKL expression by stromal cells → osteoclast activation → bone resorption. Simultaneously, myeloma factors inhibit osteoblast function. The net result: lytic lesions, hypercalcemia, pathologic fractures.
Immunosuppression
Despite elevated total immunoglobulin (from M protein), the production of functional antibodies is profoundly depressed → high susceptibility to bacterial infections.
Renal Damage
- Cast nephropathy — Bence Jones proteins (free light chains) form obstructive casts in distal tubules and collecting ducts
- Light chain deposition disease / amyloidosis — AL amyloid in glomeruli/interstitium
- Hypercalcemia → dehydration, renal stones
- Hypogammaglobulinemia → increased pyelonephritis risk
— Robbins & Kumar Basic Pathology
4. Morphology
Bone marrow aspirate (Wright-Giemsa stain, 600×) showing a predominance of plasma cells:
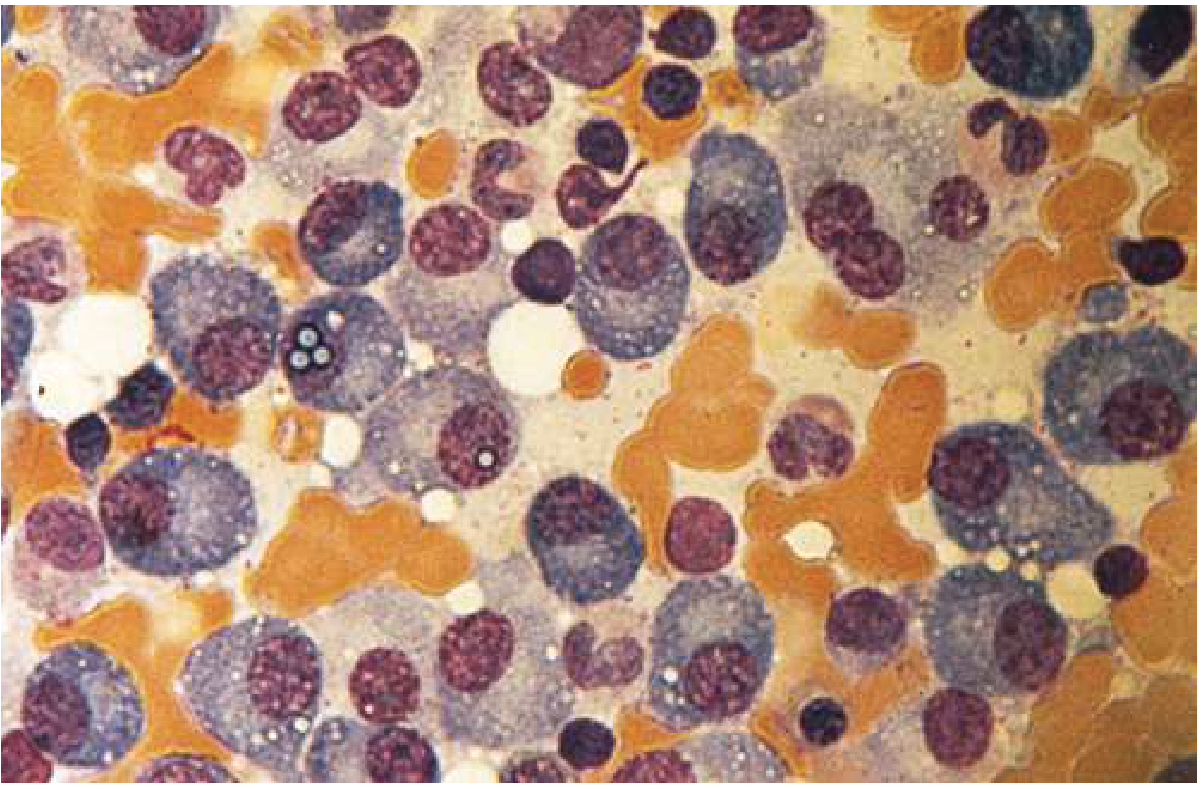
Key morphologic features:
- Cells >30% of marrow cellularity
- Eccentric nucleus with "clock-face" (cartwheel) chromatin
- Prominent nucleolus; abundant basophilic cytoplasm
- Russell bodies — cytoplasmic inclusions of condensed immunoglobulin (within distended ER)
- Occasional binucleation or multinucleation in aggressive disease
- Cells are CD138+, CD38+, CD19−, CD45−, with light chain restriction (κ or λ)
Gross pathology — vertebral lytic lesions:
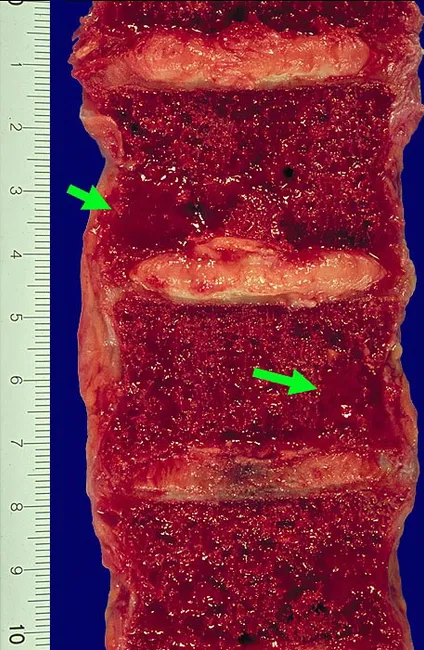
Skull X-ray — "punched-out" lytic lesions:
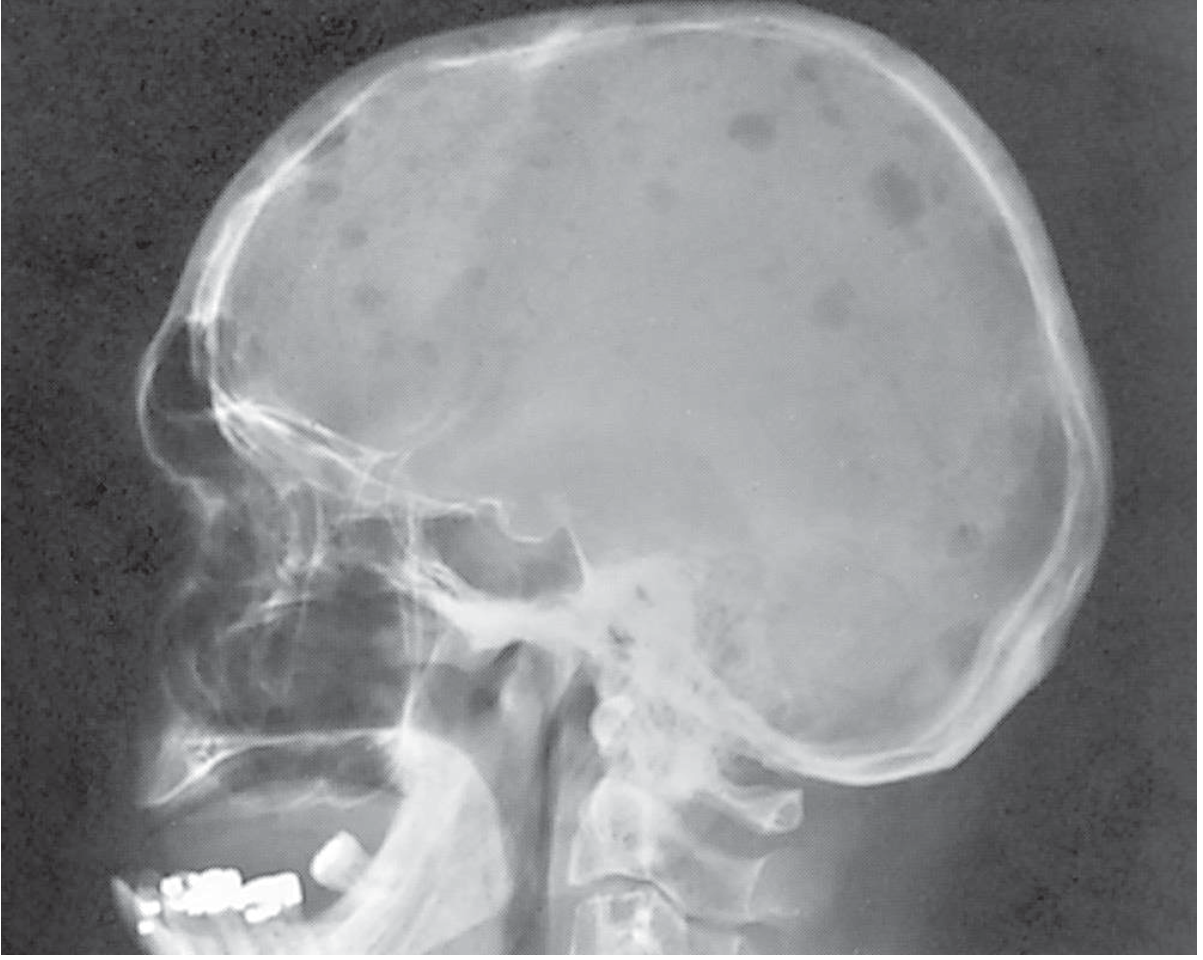
Lytic lesions (1–4 cm) most commonly involve the vertebral column, ribs, skull, pelvis, femur, clavicle, and scapula.
5. Clinical Features — CRAB
The classic mnemonic for myeloma-related end-organ damage:
| Letter | Feature | Detail |
|---|---|---|
| C | Hypercalcemia | Ca >11 mg/dL; confusion, polyuria, constipation, weakness |
| R | Renal failure | Creatinine >2 mg/dL; cast nephropathy, amyloid |
| A | Anemia | Hgb <10 g/dL; marrow replacement + erythropoietin suppression |
| B | Bone lesions | Lytic lesions, pathologic fractures, vertebral collapse, back pain |
Additional biomarker-based MDEs (even without CRAB):
- Bone marrow clonal plasma cells ≥60%
- Serum free light chain ratio ≥100 (involved/uninvolved)
- >1 focal lesion on MRI ≥5 mm
Other features: recurrent bacterial infections (especially pneumonia, UTI), fatigue, weight loss, hyperviscosity syndrome (especially IgM/IgA), peripheral neuropathy (especially with amyloid).
6. Precursor States
MGUS (Monoclonal Gammopathy of Undetermined Significance)
- M protein <3 g/dL, <10% bone marrow plasma cells, no MDE
- Risk of progression to myeloma: ~1%/year
- Low-risk MGUS (IgG, M protein <1.5 g/dL, normal FLC ratio): may require only periodic monitoring
Smoldering Multiple Myeloma (SMM)
- M protein ≥3 g/dL OR bone marrow plasma cells 10–60%, no MDE
- Higher risk of progression (~10%/year for first 5 years)
- Treatment is under active investigation
7. Diagnosis
Workup
| Test | Purpose |
|---|---|
| Serum protein electrophoresis (SPEP) | Detect M spike |
| Serum immunofixation | Type M protein (IgG, IgA, etc.) |
| Serum free light chains (sFLC) | κ/λ ratio; sensitive for nonsecretory disease |
| 24-hr urine electrophoresis + immunofixation | Detect Bence Jones protein |
| Bone marrow biopsy + aspirate | % clonal plasma cells, cytogenetics (FISH) |
| Whole-body low-dose CT or PET-CT | Lytic lesions, fracture risk (preferred over plain X-rays) |
| MRI | Focal lesions, cord compression |
| CBC, creatinine, calcium, LDH, β2-microglobulin, albumin | Organ function, staging |
| FISH cytogenetics | Risk stratification: del(17p), t(4;14), t(14;16) = high risk |
Flow cytometry of bone marrow shows the classic immunophenotype: CD38+, CD138+, CD45−, CD19−, monoclonal light chain restriction.
8. Staging
International Staging System (ISS) — Revised (R-ISS)
| Stage | Criteria | Median OS |
|---|---|---|
| I | β2-microglobulin <3.5 mg/L + albumin ≥3.5 g/dL; no high-risk FISH; normal LDH | ~Not reached (>60 mo) |
| II | Neither Stage I nor III | ~83 months |
| III | β2-microglobulin >5.5 mg/L + high-risk FISH [t(4;14), t(14;16), del(17p)] OR high LDH | ~43 months |
R2-ISS (second revision, published ~2022) adds gain(1q) as a high-risk cytogenetic feature.
9. Treatment
General Approach: Transplant-Eligible vs. Ineligible
The first key decision is whether the patient can undergo autologous stem cell transplantation (ASCT). Eligibility is primarily based on age, performance status, and organ function (not age alone).
Induction Therapy (Newly Diagnosed MM)
Per the 2025 EHA-EMN guidelines and NCCN 2025, quadruplet regimens are the new standard for transplant-eligible patients:
Transplant-eligible (preferred):
- Dara-VRd (Daratumumab + Bortezomib + Lenalidomide + Dexamethasone) — first-line standard
- Followed by ASCT, then lenalidomide maintenance
Transplant-ineligible:
- Dara-VRd or Dara-Rd (Daratumumab + Lenalidomide + Dexamethasone) — standard
- VMP (Bortezomib + Melphalan + Prednisone) — still used in frail patients
Key drug regimens from Goldman-Cecil Medicine:
| Regimen | Components | Schedule |
|---|---|---|
| VRd | Bortezomib 1.3 mg/m² IV + Lenalidomide 25 mg PO + Dexamethasone | Every 3 weeks |
| KRd | Carfilzomib + Lenalidomide + Dexamethasone | Every 4 weeks |
| Dara-Rd | Daratumumab 16 mg/kg + Lenalidomide + Dexamethasone | Weekly → biweekly → monthly |
| Dara-VRd | Daratumumab + Bortezomib + Lenalidomide + Dexamethasone | Combination |
| Elo-Rd | Elotuzumab 10 mg/kg + Lenalidomide + Dexamethasone | Every 4 weeks |
| Ixazomib-Rd | Ixazomib 4 mg PO + Lenalidomide + Dexamethasone | Every 4 weeks (all oral) |
Drug Classes
| Class | Examples | Mechanism |
|---|---|---|
| Proteasome inhibitors (PI) | Bortezomib, Carfilzomib, Ixazomib | Inhibit 26S proteasome → unfolded protein response → apoptosis |
| Immunomodulatory drugs (IMiDs) | Thalidomide, Lenalidomide, Pomalidomide | Cereblon binding → target ubiquitination → immunostimulation, anti-angiogenesis |
| Anti-CD38 monoclonal antibodies | Daratumumab, Isatuximab | Direct cytotoxicity + complement/NK cell activation |
| Anti-SLAMF7 antibody | Elotuzumab | NK cell activation |
| Alkylating agents | Melphalan, Cyclophosphamide | DNA crosslinking |
| Corticosteroids | Dexamethasone | Anti-inflammatory + direct myeloma cell apoptosis |
Autologous Stem Cell Transplantation (ASCT)
- Remains standard of care for eligible patients even in the era of novel agents
- Performed after induction (3–6 cycles)
- Conditioning: High-dose melphalan 200 mg/m²
- Single ASCT is standard; tandem ASCT in selected high-risk patients
- Maintenance with lenalidomide post-ASCT prolongs progression-free survival
Relapsed/Refractory MM
- Second-line options include Carfilzomib-Rd, Pomalidomide-based regimens, Daratumumab combinations, Elotuzumab combinations
- CAR-T cell therapies: Idecabtagene vicleucel (ide-cel) and Ciltacabtagene autoleucel (cilta-cel) — target BCMA; approved for relapsed/refractory MM (≥4 prior lines)
- Bispecific antibodies: Teclistamab (BCMA × CD3), Talquetamab (GPRC5D × CD3) — 2023–2025 approvals; now being positioned earlier in therapy per 2025 EHA-EMN guidelines
Supportive Care
| Complication | Management |
|---|---|
| Bone disease | Bisphosphonates (zoledronic acid or denosumab) monthly |
| Hypercalcemia | IV fluids, bisphosphonates, corticosteroids |
| Anemia | ESAs (erythropoietin), transfusion |
| Infections | Prophylactic antiviral (acyclovir with bortezomib), pneumococcal/influenza vaccines |
| DVT/PE (IMiD risk) | Aspirin, LMWH, or DOACs per risk stratification |
| Renal failure | Hydration, avoid NSAIDs/contrast; dose-adjusted therapy |
| Neuropathy | Dose-reduce bortezomib; switch to SC route |
| Spinal cord compression | Emergency radiation ± surgical decompression |
10. Prognosis
| Factor | Favorable | Unfavorable |
|---|---|---|
| Cytogenetics | Trisomies, t(11;14) | del(17p), t(4;14), t(14;16), gain(1q) |
| R-ISS Stage | I | III |
| LDH | Normal | Elevated |
| β2-microglobulin | <3.5 mg/L | >5.5 mg/L |
| Serum albumin | ≥3.5 g/dL | <3.5 g/dL |
| Plasma cell % at diagnosis | <60% | ≥60% |
With modern quadruplet therapy and ASCT, median OS for transplant-eligible patients now exceeds 7–10 years in many trials. Standard-risk patients may achieve median OS >10 years, while high-risk patients remain a challenge.
The disease is currently incurable in the vast majority of patients, though a small fraction (possibly those achieving MRD-negative sustained remissions) may experience functional cure.
11. Prevention
There is no established proven prevention strategy for multiple myeloma, as its etiology is largely unknown. However, evidence points to several modifiable risk factors and surveillance strategies:
Known/Suspected Risk Factors
| Factor | Evidence |
|---|---|
| Age >65 | Non-modifiable; greatest risk factor |
| African descent | Non-modifiable; 2× higher incidence |
| Male sex | Non-modifiable |
| Obesity | Associated with increased risk; weight management may reduce risk |
| Radiation exposure | Ionizing radiation (e.g., atomic bomb survivors) — limit unnecessary exposure |
| Occupational exposures | Pesticides, benzene, dioxins, Agent Orange — minimize industrial chemical exposure |
| Family history | First-degree relatives have ~2–3× increased risk |
| MGUS → MM progression | Annual risk ~1%; surveillance detects early conversion |
Prevention Strategies
-
Surveillance of MGUS — The most actionable prevention tool. Regular monitoring (SPEP, FLC, CBC) every 6–12 months detects progression to SMM or active MM early, enabling timely treatment initiation before severe end-organ damage.
-
SMM intervention trials — Clinical trials (e.g., QUIREDEX, GEM-CESAR, E3A06/ECOG) are investigating whether early treatment of high-risk SMM can prevent or delay progression to active myeloma. Lenalidomide-based therapy has shown progression-free survival benefit in high-risk SMM.
-
Maintain healthy weight — Obesity is a recognized modifiable risk factor; BMI management may reduce lifetime risk.
-
Avoid known carcinogens — Occupational hygiene for benzene, pesticides, and solvents; proper radiation safety.
-
No chemoprevention agent is currently approved or recommended for primary prevention.
-
Vaccination and infection prevention — While not preventive of myeloma itself, patients with MGUS should maintain up-to-date vaccinations (pneumococcal, influenza, COVID-19, Hib) because immunoparesis exists even at the precursor stage.
Summary Table
| Domain | Key Points |
|---|---|
| Definition | Clonal plasma cell malignancy; ≥10% BM plasma cells + M protein + MDE |
| Epidemiology | 30,000 US cases/year; median age 70; more common in men and Black patients |
| Pathogenesis | IgH translocations, cyclin dysregulation, IL-6, RANKL-mediated bone destruction |
| Morphology | Plasma cells with Russell bodies, punched-out lytic bone lesions |
| Clinical | CRAB criteria + infections + neuropathy |
| Diagnosis | SPEP, immunofixation, FLC, bone marrow biopsy, FISH, whole-body CT/PET |
| Staging | R-ISS (β2-M, albumin, LDH, FISH) |
| Treatment | Quadruplet induction (Dara-VRd) → ASCT → lenalidomide maintenance; CAR-T/bispecifics for relapse |
| Prognosis | Incurable but increasingly manageable; median OS 7–10+ years with modern therapy |
| Prevention | No proven primary prevention; MGUS surveillance; BMI control; avoid carcinogens |
Sources:
- Goldman-Cecil Medicine International Edition, Chapter 173 (Plasma Cell Disorders)
- Robbins & Kumar Basic Pathology, Chapter 10 (Lymphoid Neoplasms)
- EHA-EMN 2025 Evidence-Based Guidelines for Multiple Myeloma (Nature Reviews Clinical Oncology)
- NCCN Guidelines Version 1.2025 — Multiple Myeloma
Can u explain this as simple as it is ,like to a child, adult in a story format , u can even tell the story in tamil, like a narrative as a active learning
🦴 Multiple Myeloma — ஒரு கதை வழி கற்கலாம்!
A Story in Tamil + English — Told Like a Narrative for Active Learning
🏘️ முதலில் — நம் உடலின் "காவல் நகரம்" (Our Body's Defense City)
உங்கள் உடலை ஒரு பெரிய நகரம் என்று நினைத்துக்கொள்ளுங்கள்.
அந்த நகரில் ஒரு சிறப்பு படை இருக்கிறது — Plasma Cells என்னும் வீரர்கள்.
These are your plasma cells — special soldiers made inside your bone marrow (எலும்பின் உள்ளே இருக்கும் மென்மையான பகுதி — like the spongy center of your bones).
இந்த வீரர்களின் வேலை என்ன?
நோய்க்கிருமிகள் வரும்போது — antibodies என்னும் அம்புகளை எய்வது!
ஒவ்வொரு plasma cell-உம் ஒரு திறமையான வில்லாளி. சரியான நேரத்தில், சரியான அளவில் அம்பு எய்வான்.
😈 பிறகு என்ன ஆயிற்று? — The Villain Enters
ஒரு நாள்...
நகரத்தில் ஒரு வீரன் "கெட்டவனாக" மாறுகிறான்.
அவன் திடீரென்று பைத்தியக்காரனாக வளர ஆரம்பிக்கிறான் — நிறுத்தவே மாட்டான்!
This is what happens in Multiple Myeloma — one plasma cell goes rogue. It starts multiplying uncontrollably inside the bone marrow. Instead of one soldier, now there are thousands of broken, useless copies — all clones of that one bad cell.
அந்த கெட்ட வீரனின் பெயர்: Myeloma Cell 🦹
🏚️ கெட்ட வீரன் என்ன செய்கிறான்? — What Does He Destroy?
இப்போது நகரத்தில் கெட்ட வீரர்கள் நிறைந்துவிட்டார்கள். அவர்கள் நான்கு இடங்களை நாசமாக்குகிறார்கள்:
🦴 1. எலும்புகளை உடைக்கிறான் — Bone Destruction
Imagine your bones are like walls of a fort. The myeloma cells send out signals that say: "Break the walls! Break the walls!"
உடலில் Osteoclast என்னும் "wall-breaker" செல்கள் இருக்கின்றன — இவை பொதுவாக பழைய எலும்பை மெதுவாக உடைத்து புதியது கட்டும்.
ஆனால் myeloma cells இந்த wall-breakerகளை மிகவும் வேகமாக, மிகவும் அதிகமாக வேலை செய்ய வைக்கின்றன.
முடிவு:
- Bones become fragile → pathologic fractures (சின்ன காரணத்திற்கே எலும்பு உடையும்)
- எலும்பிலிருந்து calcium ரத்தத்தில் கரைந்து போகும் → Hypercalcemia (அதிக calcium in blood)
நோயாளிக்கு முதுகு வலி, எலும்பு வலி மிகவும் அதிகமாக இருக்கும்.
🩸 2. நல்ல ரத்த செல்களை ஓட்டுகிறான் — Anemia
The bone marrow is like a factory that makes blood cells. But now the factory is so full of myeloma cells — there's no space to make normal red blood cells!
முடிவு: Anemia — சோர்வு, மூச்சு வாங்குதல், வெளிர் தோல்.
🧱 3. சிறுநீரகத்தை அடைக்கிறான் — Kidney Damage
Myeloma cells உதவாத, broken antibody pieces (Bence Jones proteins / free light chains) ரத்தத்தில் கொட்டுகின்றன.
Think of it like a factory that produces broken toy parts — they clog up the city's drainage pipes.
Kidney = drainage system of the body.
இந்த broken pieces சிறுநீரக குழாய்களை அடைக்கின்றன → Renal failure.
🦠 4. நோய் எதிர்ப்பு சக்தியை அழிக்கிறான் — Immunosuppression
The myeloma cells are making a LOT of useless antibodies — like spam mail filling your inbox. Real important mail (real antibodies) can't get through.
முடிவு: நோயாளிக்கு மீண்டும் மீண்டும் தொற்று நோய்கள் (bacterial infections) வரும் — Pneumonia, UTI.
🔤 CRAB — நான்கு அழிவின் அடையாளம்
இந்த நான்கு damage-ஐ டாக்டர்கள் ஒரு எளிய வார்த்தையால் நினைவில் வைக்கிறார்கள்:
| எழுத்து | ஆங்கிலம் | தமிழ் |
|---|---|---|
| C | Calcium elevated | அதிக Calcium — குழப்பம், தாகம், மலச்சிக்கல் |
| R | Renal failure | சிறுநீரகம் செயல் இழப்பு |
| A | Anemia | ரத்தம் குறைவு — சோர்வு |
| B | Bone lesions | எலும்பு துளைகள் — வலி, உடைவு |
நினைவு வாசகம்: "CRAB வந்தால் — Myeloma நினைவில் வையுங்கள்!"
🔬 டாக்டர் எப்படி கண்டுபிடிக்கிறார்? — Diagnosis, Simplified
கதை தொடர்கிறது...
60 வயது Rajan uncle-க்கு திடீரென்று முதுகு வலி வருகிறது. சோர்வு அதிகமாகிறது. ரத்த பரிசோதனையில் calcium அதிகமாக இருக்கிறது.
டாக்டர் சந்தேகப்படுகிறார்: "இது Myeloma-ஆ இருக்குமோ?"
பரிசோதனைகள்:
🔍 ரத்த பரிசோதனை (SPEP)
→ ரத்தத்தில் "M protein" என்னும் கெட்ட antibody spike தெரிகிறது
🔍 சிறுநீர் பரிசோதனை
→ "Bence Jones protein" — broken light chains
🔍 Bone Marrow Biopsy
→ எலும்பு ஊட்டில் 40% myeloma cells!
(Normal = <5%)
🔍 Skull X-ray / Full body CT
→ "Punched-out" lytic lesions —
தலையோட்டில் துளைகள் போல் காணப்படும்!
🔍 FISH Cytogenetics
→ del(17p) கண்டுபிடித்தார்கள் — High risk!
Diagnosis confirmed: Multiple Myeloma, R-ISS Stage III.
💊 சிகிச்சை — The Battle Plan
Now the doctors become generals. They need a strategy to fight the myeloma army.
படை 1: மருந்துகள் — Drug Regimens
மூன்று வகை வீரர்கள் மருந்தில் இருக்கிறார்கள்:
| மருந்து வகை | பெயர் | என்ன செய்யும்? |
|---|---|---|
| Proteasome Inhibitor | Bortezomib (Velcade) | Myeloma cellன் "குப்பை disposal system"-ஐ அடைக்கும் → Cell சாகும் |
| IMiD | Lenalidomide (Revlimid) | Immune system-ஐ activate செய்யும் + myeloma-ஐ அழிக்கும் |
| Monoclonal Antibody | Daratumumab (Darzalex) | CD38 என்னும் myeloma cell-ன் "uniform"-ஐ பிடித்து அழிக்கும் |
| Steroid | Dexamethasone | Inflammation குறைக்கும் + myeloma cells-ஐ kill செய்யும் |
Standard regimen: Dara-VRd
= Daratumumab + Bortezomib + Lenalidomide + Dexamethasone
(2025 EHA-EMN guideline — புதிய standard of care)
படை 2: Stem Cell Transplant 🔄
After chemotherapy kills most myeloma cells... doctors do a "factory reset" of the bone marrow.
- முதலில் patient-ன் சொந்த stem cells சேகரிக்கப்படுகின்றன (harvest)
- பிறகு high-dose melphalan கொடுத்து bone marrow-ஐ முழுவதும் "clean" செய்கிறார்கள்
- பின்பு சொந்த stem cells திரும்ப உட்செலுத்தப்படுகின்றன
- New, healthy bone marrow மீண்டும் கட்டமைக்கப்படுகிறது
இதுவே Autologous Stem Cell Transplantation (ASCT) — நவீன சிகிச்சையின் முக்கிய படி.
படை 3: CAR-T Cell Therapy 🚀 (புதிய ஆயுதம்!)
Doctors take YOUR OWN immune cells, re-program them in a lab like Iron Man's suit, then put them back — now they can find and kill myeloma cells with laser precision.
இது CAR-T therapy — Relapsed/Refractory Myeloma-க்கு approved.
(Ide-cel, Cilta-cel — BCMA target)
📊 Staging — எந்த நிலையில் இருக்கிறோம்?
Think of it like levels in a video game.
| Stage | என்ன இருக்கும்? | Survival |
|---|---|---|
| I | β2-microglobulin குறைவு, albumin சரி, No bad genetics | 60+ months |
| II | நடுவில் | ~83 months |
| III | β2-microglobulin அதிகம் + Bad genetics (del 17p) + High LDH | ~43 months |
🌱 Prevention — தடுக்க முடியுமா?
நேர்மையான பதில்: முழுமையாக தடுக்க முடியாது.
ஆனால் — ஆபத்தை குறைக்கலாம்:
🧓 MGUS என்பது ஒரு "pre-crime" நிலை — Myeloma வருவதற்கு முன்பு ஒரு சின்ன signal.
MGUS (Monoclonal Gammopathy of Undetermined Significance) என்பது:
- Myeloma இல்லை
- ஆனால் ஒரு கெட்ட plasma cell குடும்பம் ஆரம்பித்திருக்கிறது
- வருடத்தில் ~1% மட்டுமே myeloma-ஆக மாறும்
ஆகவே MGUS கண்டுபிடித்தால்:
→ 6–12 மாதத்திற்கு ஒரு முறை monitoring (blood test, SPEP, FLC)
→ ஏதாவது CRAB signs வந்தால் — உடனே doctor-கிட்டே போகணும்!
Prevention checklist:
| என்ன செய்யலாம்? | ஏன்? |
|---|---|
| ✅ உடல் எடை கட்டுப்படுத்துங்கள் | Obesity = higher MM risk |
| ✅ Pesticides, benzene தொடர்பை தவிர்யுங்கள் | Known carcinogens |
| ✅ MGUS இருந்தால் — regular checkup | Catch progression early |
| ✅ Vaccines போடுங்கள் (Pneumococcal, Flu) | MGUS-லேயே immunity கொஞ்சம் குறைவு |
| ✅ Radiation exposure குறைத்துக்கொள்ளுங்கள் | Ionizing radiation is a risk factor |
| ❌ Primary prevention drug இல்லை | Research ongoing |
🎬 கதையின் முடிவு — The Story So Far
Normal Plasma Cell
↓ (mutation)
Bad Clone → Multiplies → MGUS
↓ (progression)
Smoldering Myeloma
↓ (progression)
Active Multiple Myeloma
→ CRAB symptoms
→ Diagnosis (SPEP, BM biopsy, imaging)
→ Staging (R-ISS)
→ Treatment (Dara-VRd → ASCT → Maintenance)
→ Relapse → CAR-T / Bispecifics
↓
Managed, but currently incurable
(Research toward cure is ongoing 🔬)
🧠 Active Learning — நீங்களே சோதியுங்கள்!
Quick Quiz (விடை மனசில் யோசியுங்கள்):
- 🤔 Myeloma Cell எந்த normal cell-லிருந்து வருகிறது?
- 🤔 CRAB-ல் "R" என்றால் என்ன?
- 🤔 Bone marrow-ல் plasma cells எத்தனை % இருந்தால் Myeloma diagnose செய்வார்கள்?
- 🤔 Bortezomib எந்த pathway-ஐ block செய்கிறது?
- 🤔 Myeloma-ல் எலும்பு உடைவதற்கு காரணமான cell என்ன?
(விடைகள் மேலே கதையில் இருக்கின்றன — திரும்பி படியுங்கள்!)
Bottom line: Multiple Myeloma என்பது ஒரு கெட்ட plasma cell-ன் கதை — அது எலும்பை உடைக்கிறது, சிறுநீரகத்தை அழிக்கிறது, நோய் எதிர்ப்பை கெடுக்கிறது. ஆனால் இன்றைய மருத்துவம் — Dara-VRd, ASCT, CAR-T — இந்த கெட்ட கதைக்கு நல்ல எதிர்ப்பை தருகிறது. 💪
Myelodysplastic explain everything from the word to end
Reading File
Your credits are exhausted. Your daily credits reset tomorrow, or you can purchase a top-up for more.
This is a shared conversation. Sign in to Orris to start your own chat.