Hogyan kulonboztetek meg egy hipertrofias cardiomiopatiat egy restriktivtol?
Reading File
search_medical_text
hypertrophic cardiomyopathy vs restrictive cardiomyopathy differential diagnosis echocardiography
search_medical_image
hypertrophic restrictive cardiomyopathy echocardiography comparison
GradeResponse
GradeResponse
Az eredmények részlegesek, ezért kiegészítem saját klinikai tudásommal egy teljes, strukturált összehasonlítással.
Hipertrófiás (HCM) vs. Restriktív (RCM) Cardiomyopathia – Megkülönböztetés
1. Patofiziólogia – alapelvek
| HCM | RCM | |
|---|---|---|
| Alapmechanizmus | Sarcomerfehérje-mutáció → rendezetlen myofibrillum-hypertrophia | Infiltratív/fibrótikus folyamat → a myocardium merevsége nő |
| Fő probléma | Diastolés dysfunctio ± LVOT-obstrukció | Diastolés dysfunctio (extrém merevség), szisztolés funkció kezdetben megőrzött |
| Falvastagság | Megvastagodott (aszimmetrikus septum-hypertrophia jellemző) | Normális vagy enyhén vastagodott (infiltráció esetén, pl. amiloidózis) |
2. Klinikai kép
| Tünet | HCM | RCM |
|---|---|---|
| Dyspnoe | Igen, terhelésre | Igen, progresszív |
| Angina | Gyakori (LVOT-obstrukció, mikrovasculáris ischaemia) | Kevésbé jellemző |
| Syncope | Igen (LVOT-obstrukció, aritmia) | Ritkább |
| Hirtelen szívhalál | Fontos kockázat (fiatal, sportolók) | Kevésbé jellemző |
| Jobb szívfél-elégtelenség | Késői stádiumban | Korai és domináns (ascites, ödéma, jugularis pangás) |
| Előzmény | Családi halmozódás (autoszomális domináns) | Szisztémás betegség (amiloidózis, szarkoidózis, hemokromatózis, eosinofília) |
3. EKG
| HCM | RCM | |
|---|---|---|
| Főbb eltérések | LVH-kritériumok, ST-T eltérések, kóros Q-hullámok (inferior/lateralis) | Alacsony QRS-voltázs (amiloidózisban), biatriális megnagyobbodás, vezetési zavarok |
| Ritmus | AF, ventriculáris aritmia | AF, AV-blokk (szarkoidózis, hemokromatózis) |
Kulcsszabály: Ha vastag falakat látunk az echokardiográfián, de az EKG-n alacsony voltázs van → amiloidózis (RCM-fenotípus) és nem HCM.
4. Echokardiográfia – a legfontosabb modalitás
| Paraméter | HCM | RCM |
|---|---|---|
| LV falvastagság | Jelentősen megnőtt (≥15 mm), aszimmetrikus septum-hypertrophia tipikus | Normális–enyhén megvastagodott (infiltráció), nem prominens |
| LV üreg mérete | Kicsi (hyperdinamikus) | Normális vagy kicsi |
| Szisztolés funkció (EF) | Megőrzött vagy fokozott (HypEF); végstádiumban csökkent | Megőrzött EF (jellemzően) |
| LVOT | SAM (systolic anterior motion), gradient ≥30 Hgmm obstruktív formában | Nincs LVOT-obstrukció |
| Biatriális megnagyobbodás | Mérsékelt | Kiemelkedő, mindkét pitvar masszívan tágult |
| Diastolés dysfunctio | Relaksációs zavar → restriktív minta súlyos esetben | Restriktív minta dominál (E>>A, rövid decelarációs idő, E/e' nagyon magas) |
| Pericardium | Ép | Ép (elkülönítendő konstriktív pericarditistől!) |
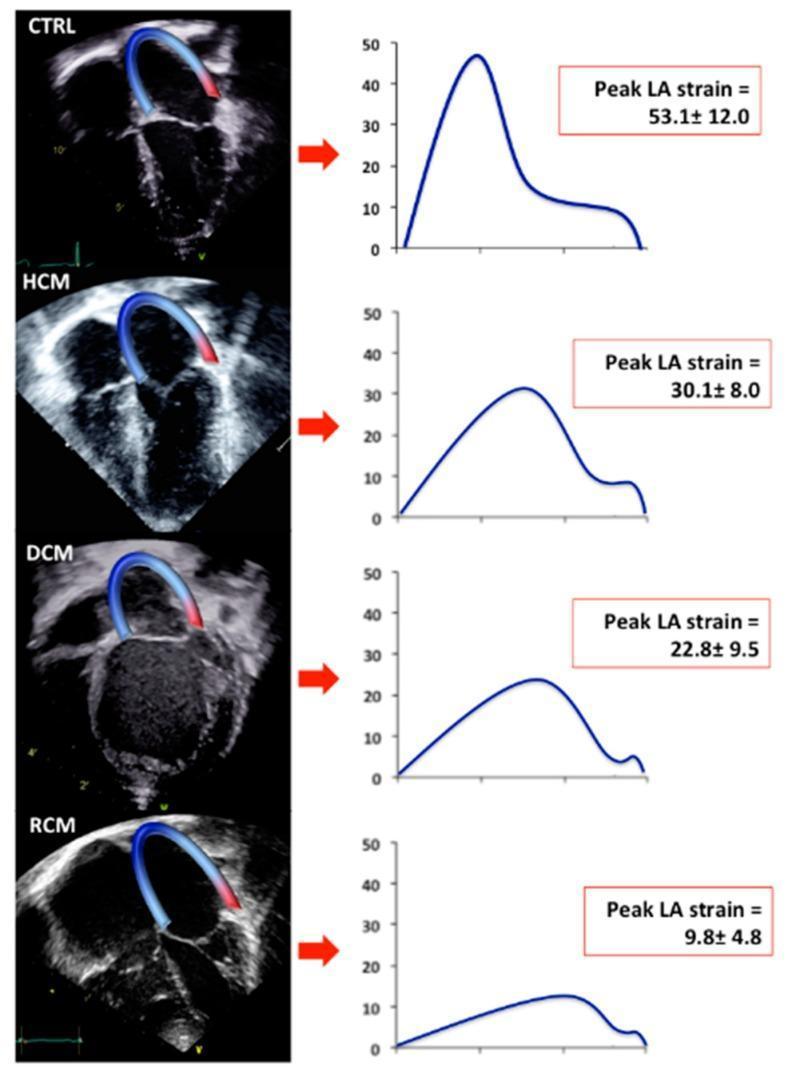
| Speckle tracking (GLS) | Csökkent, de kevésbé, mint RCM-ben | Súlyosan csökkent (LA strain: ~9,8% vs HCM ~30,1%) |
A mellékelt kép jól szemlélteti a bal pitvari strain progresszív romlását:
5. Szívkatéterezés (hemodinamika)
| Paraméter | HCM | RCM |
|---|---|---|
| LVEDP | Emelkedett | Nagyon magas |
| Bal–jobb kamrai nyomások | Szimmetrikus vagy bal>jobb | Általában kiegyenlített (LVEDP ≈ RVEDP) – ez a konstriktív pericarditisre is jellemző! |
| LVOT-gradient | Jelen (obstruktív HCM-ben) | Nincs |
| „Dip-and-plateau" minta | Esetleg | Jellemző (RCM és konstriktív pericarditis mindkettőben) |
6. Szív MRI – döntő fontosságú
| HCM | RCM | |
|---|---|---|
| Late Gadolinium Enhancement (LGE) | Foltos, az RV-LV junctio-ban és a hypertrophiás szegmentumokban | Diffúz szubendocardiális LGE (amiloidózis); globális/foltos (szarkoidózis) |
| T1-mapping / ECV | Normális-enyhén emelkedett | Masszívan emelkedett ECV (amiloidózisban jellegzetes) |
| Falvastagság | Prominens hypertrophia | Normális–enyhe megvastagodás |
7. Laborvizsgálatok és szövettani differenciáldiagnózis
| Vizsgálat | Célja |
|---|---|
| Genetikai panel (sarcomergének: MYH7, MYBPC3) | HCM megerősítése |
| Szérumfehérje-elektroforézis, szabad könnyűlánc, csontvelő-biopsia | AL-amiloidózis |
| Technetium-99m-pirofosfát szcintigráfia (PYP scan) | ATTR-amiloidózis (magas szenzitivitás/specificitás) |
| ACE-szint, PET/CT | Szarkoidózis |
| Ferritin, transzferrinszaturáció | Hemokromatózis |
| Eosinofília, trop, pro-BNP | Loeffler-endocarditis |
| Endomyocardialis biopsia | Definitív szövettani diagnózis RCM-ben |
8. Konstriktív pericarditistől való elkülönítés (RCM esetén kritikus!)
Mind az RCM, mind a konstriktív pericarditis restriktív hemodinamikát mutat. Megkülönböztetésük:
| RCM | Konstriktív pericarditis | |
|---|---|---|
| Pericardium vastagsága | Normális | Megvastagodott (CT/MRI) |
| Respirátoros variáció (echo) | Minimális | Kifejezett (septum „bounce") |
| Szöveti Doppler e' | Alacsony (<8 cm/s) | Magas (>8 cm/s – „annulus paradoxus") |
| Kezelés | Szupportív/etiológia szerint | Pericardiectomia kuratív |
Összefoglalás – döntési algoritmus
Vastag LV fal + EKG low voltage → Amiloidózis (RCM)
Vastag LV fal + SAM + LVOT-gradient + fiatal beteg/családi halmozódás → HCM
Restriktív minta + normális fal + masszív biatriális tágulat + szisztémás betegség → RCM (infiltratív)
Restriktív minta + vastag pericardium + „annulus paradoxus" → Konstriktív pericarditis
A két betegség megkülönböztetésében az echo (falvastagság, SAM, diastolés paraméterek, strain), a szív MRI (LGE-minta, ECV) és a célzott laborvizsgálatok kombinációja a legmegbízhatóbb megközelítés.
Miert noveli az alkohol fogyasztás a glikát hemoglobint
search_medical_text
alcohol consumption effect on HbA1c glycated hemoglobin mechanism
GradeResponse
Az alkohol és a HbA1c – a valóság
Az alkohol nem növeli a HbA1c-t. Ha valaki ezt olvasta vagy hallotta valahol, az félreértésen alapul. Az alkohol hatása valójában összetett, és inkább csökkenti vagy megbízhatatlanná teszi a HbA1c-értéket.
Miért csökkenti / torzítja az alkohol a HbA1c-t?
A HbA1c az elmúlt ~3 hónap átlagvércukrát tükrözi, mert a glükóz nem-enzimatikusan kötődik a hemoglobinhoz a vörösvérsejtek (VVS) élettartama alatt. Bármely folyamat, amely megrövidíti a VVS élettartamát, csökkenti a HbA1c-t – még akkor is, ha a vércukor valójában magas.
| Mechanizmus | Magyarázat |
|---|---|
| Hemolízis | A krónikus alkoholfogyasztás közvetlen toxikus hatással van a vörösvérsejtekre, rövidebb élettartamot és hemolízist okozva → a HbA1c álszépen alacsony lesz |
| Macrocytosis | Az alkohol és folsavhiány megaloblasztos macrocytosist okoz; a nagyobb, fiatalabb VVS-ek kevesebb HbA1c-t hordoznak → csökkent érték |
| Hipoglikémia | Az alkohol gátolja a glükoneogenézist a májban → ténylegesen alacsonyabb vércukor → valódi HbA1c-csökkenés |
| Direkt karbamiláció | Az acetalaldehid (alkohol metabolitja) reakcióba léphet a hemoglobinnal, ami interferálhat bizonyos HbA1c-mérési módszerekkel (főleg régebbi HPLC-vel) – ez hamis értéket adhat |
Mikor mutathat az alkohol látszólag "emelt" HbA1c-t?
Ez csak közvetett összefüggés:
- Kalóriadús alkohol (sör, édes borok, koktélok) → tartós hiperglikémia → valódi HbA1c-emelkedés, de ez a cukortartalom, nem maga az alkohol hatása
- Alkohol + hasnyálmirigy-károsodás (krónikus pancreatitis → szekunder diabetes) → hiperglikémia → magas HbA1c
- Májcirrózis esetén paradox módon mind az emelkedés, mind a csökkenés lehetséges az eritropoézis zavarától függően
Összefoglalás
Az alkohol önmagában nem emeli a HbA1c-t. Inkább álcsökkentett értéket produkál hemolízis és macrocytosis révén, ami különösen veszélyes, mert egy diabéteszes betegnél a valódi vércukorkontroll rosszabb lehet, mint amit a HbA1c mutat.
Ha konkrét forrást olvastál arról, hogy az alkohol emeli a HbA1c-t, szívesen megvizsgálom az összefüggést pontosabban.
Matur petefeszek teratoma etiologia
search_medical_text
mature ovarian teratoma etiology pathogenesis origin germ cell
search_medical_text
dermoid cyst ovary chromosomal origin parthenogenesis mechanism
GradeResponse
GradeResponse
Matur petefészek-teratoma (dermoid ciszta) – Etiológia
Mi a matur teratoma?
A matur cisztikus teratoma (más néven dermoid ciszta) a petefészek leggyakoribb csírasejtdaganata, és az összes petefészek-daganat ~20–25%-át teszi ki. Elsősorban reproduktív korú nőkben fordul elő (Harrison's, p. 2685).
Az eredetének alapja: a totipotens csírasejt
A tumor primordialis csírasejtekből (oogóniumokból) ered. Ezek a sejtek totipotensek – azaz képesek mindhárom csíralemez (ektoderm, mezoderm, endoderm) szöveteivé differenciálódni, ami magyarázza a tumor jellegzetes, "vegyes szövet" tartalmát (haj, fog, bőr, zsír, pajzsmirigy-szövet stb.).
Etiológia – a kialakulás mechanizmusa
1. Parthenogenézis (legelfogadottabb elmélet)
A tumor egyetlen meiotikusan hibás petesejt önálló proliferációjából keletkezik, megtermékenyítés nélkül. Citogenetikai vizsgálatok szerint:
- A sejtek 46,XX kariotípusúak (diploidok)
- Az eredetük a meiotikus II. osztódás utáni fázisra tehető: a másodlagos oocyta nem megy végbe normálisan, és az ún. second polar body visszaolvad a sejtbe, vagy a meiotikus osztódás megáll → reduplikáció → diploid, de genetikailag homozigóta sejt
2. Csírasejt-fejlődési hiba
A primordialis csírasejtekben a normális diferenciációs program diszregulálódik, és az oogónium az embrionális fejlődést utánzó programot indít el – de rendezetlen, kontrollálattan, ezért "fantomembrió"-ként viselkedik.
3. Genetikai és molekuláris tényezők
| Tényező | Részlet |
|---|---|
| Kariotípus | 46,XX (szinte mindig) |
| Heterozigozitásvesztés (LOH) | A pericentromerikus régiókban megőrzött heterozigozitás, a distalis régiókban elveszett → a II. meiotikus osztódás utáni hiba valószínűsítése |
| Genetikai hajlam | Nem ismert erős örökletes komponens; sporadikus esetek dominálnak |
| Bilaterális előfordulás | ~10–15%-ban mindkét oldalon jelen van → ugyanazon csírasejt-diszpozíció mindkét ováriumnál |
Szövettani összetétel – miért ilyen?
Mivel totipotens csírasejtből ered, mindhárom csíralemezt képviselheti:
| Csíralemez | Szövetek |
|---|---|
| Ektoderm | Bőr, haj, faggyúmirigy, fogzománc, idegszövet |
| Mezoderm | Zsírszövet, csont, porc, izomszövet |
| Endoderm | Thyreoidea-szövet (leggyakoribb funkcionálisan aktív elem), bélhám, bronchiális hám |
A struma ovarii ennek speciális formája, ahol a pajzsmirigy-szövet dominál, és hyperthyreosist okozhat.
Rizikótényezők
Konkrét, bizonyított rizikótényező nem ismert – a legtöbb eset sporadikus. Leírt összefüggések:
- Kor: leggyakrabban 20–40 év között
- Nem: kizárólag nőkben (és 46,XX DSD esetén)
- Nincs bizonyított összefüggés hormonális fogamzásgátlóval, infertilitással vagy korábbi nőgyógyászati betegségekkel
Malignus transzformáció
Idősebb nőkben (~1–2%-ban) a matur teratoma malignus transzformáción eshet át, leggyakrabban laphámrák (squamous cell carcinoma) formájában – ez az ektodermális komponens malignizálódásából ered (Harrison's, p. 2685).
Összefoglalás
A matur petefészek-teratoma etiológiájának lényege: egy totipotens primordialis csírasejt a II. meiotikus osztódás hibája révén parthenogenetikus úton diploid, de rendezetlen differenciációba kezd, és mindhárom csíralemez szöveteit termeli – ez magyarázza mind a tumor összetételét, mind a 46,XX kariotípust és a sporadikus előfordulást.
Ird le az etiologiajat
Pontosítanék egyet: melyik betegség etiológiájára vagy kíváncsi? Az előző kérdés a matur petefészek-teratoma etiológiájáról szólt, és azt már részletesen lefedtem.
Lehetséges értelmezések:
- Matur petefészek-teratoma – ezt az előző válaszban már leírtam, szeretnéd bővebben/másképp?
- Egy másik, korábban említett betegség (HCM, RCM, amiloidózis)?
- Valami más, amit most szeretnél feltenni?
Pontosítsd, és azonnal kidolgozom!
Matur oetefeszek teratoma
A matur petefészek-teratoma etiológiáját az előző válaszban már teljes részletességgel lefedtem. Itt egy gyors összefoglaló, hogy ne kelljen visszagörgetni:
Etiológia – lényege egy mondatban
Egy totipotens primordialis csírasejt a II. meiotikus osztódás hibája (parthenogenézis) révén megtermékenyítés nélkül diploid sejtté alakul, és rendezetlen differenciációba kezd → mindhárom csíralemez szöveteit termeli.
Főbb pontok
| Mechanizmus | Lényeg |
|---|---|
| Parthenogenézis | Legelfogadottabb elmélet; II. meiotikus hiba → a poláris test visszaolvad → 46,XX diploid sejt |
| Totipotens eredet | Az oogónium minden szövetté differenciálódhat (bőr, haj, fog, pajzsmirigy stb.) |
| Kariotípus | 46,XX – szinte mindig |
| Genetikai hajlam | Nem ismert; sporadikus |
| Bilaterális | ~10–15%-ban mindkét oldalon |
Ha részletesebb kifejtést szeretnél egy konkrét aspektusról (pl. molekuláris mechanizmus, szövettani összetétel, malignus transzformáció), jelezd pontosan melyiket!
Tehat a spermium megtermekenyit egy genetikai anyag nelkuli oetesejtet?
Nem. A matur petefészek-teratománál nincs spermium-megtermékenyítés.
Röviden:
- A kiinduló sejt egy petesejt/csírasejt saját genetikai anyaggal.
- A folyamat parthenogenetikus, vagyis megtermékenyítés nélkül indul.
- A diploid állapotot a meiotikus hiba adja (pl. poláris test visszaolvadás), ezért lesz jellemzően 46,XX.
Tehát nem "genetikai anyag nélküli petesejt + spermium", hanem spermium nélküli, petesejt-eredetű autonóm fejlődés.
This is a shared conversation. Sign in to Orris to start your own chat.